Newsletter
auf den Punkt. 5/2021
24.06.2021
Geltungsbeginn der MDR – und jetzt?
Zu Beginn der Corona-Pandemie im vergangenen Jahr wurde der Geltungsbeginn der neuen EU-Verordnung über Medizinprodukte (MDR) um ein Jahr verschoben, um Versorgungsengpässe bei wichtigen Medizinprodukten während der Pandemie zu verhindern. Denn die MDR verlangt auch für alle Bestandsprodukte eine neue Konformitätsbewertung auf Basis der MDR. Da aber auch drei Jahre nach Verabschiedung der MDR nicht genügend Benannte Stellen für die MDR notifiziert waren, wären einige Produkte vielleicht nicht mehr am Markt verfügbar gewesen. Durch den verschobenen Geltungsbeginn wurde das verhindert
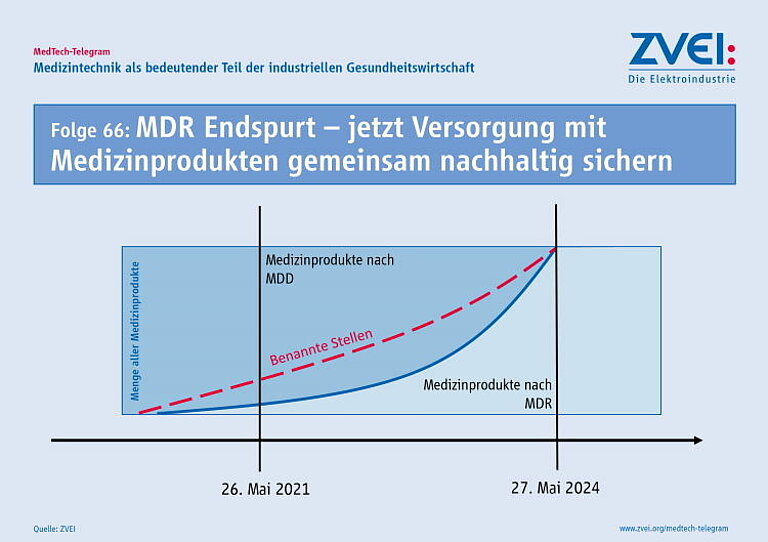
Seit dem 26. Mai 2021 ist die MDR nun gültig. Allerdings sind fast alle offenen Probleme, die vor einem Jahr beklagt wurden, weiterhin vorhanden. Zu wenige Benannte Stellen, fehlende Rechtsakte zur Umsetzung und fehlende Leitfäden zu bestimmten Anforderungen. Drohen also jetzt Versorgungsengpässe bei Medizinprodukten?
Die Antwort ist Nein. Aber es droht eine Belastung der Wettbewerbsfähigkeit der europäischen Medizinproduktebranche. Für Bestandsprodukte gelten in den nächsten zwei Jahren noch Übergangsregelungen, wenn für diese Produkte gültige Zertifikate nach der bisher gültigen Medizinprodukte-Richtlinie (MDD) vorliegen. Aber für alle wesentlichen Weiterentwicklungen von Bestandsprodukten und für alle neu entwickelten Produkte ist eine CE-Kennzeichnung nach der MDR notwendig. Da es weiter zu wenig Benannte Stellen gibt, die diese Konformitätsbewertung durchführen dürfen, stockt dieser Prozess. Innovative Produkte können also in der EU nur schwer auf den Markt gebracht werden. Hinzu kommt: Wenn in den nächsten beiden Jahren die Gültigkeit sämtlicher MDD-Zertifikate abläuft, wird der Andrang bei den Benannten Stellen noch zunehmen. Der ZVEI setzt sich deshalb für pragmatische Lösungen in diesen Punkten ein. Eine flexible Betrachtung von Bestandsprodukten und Medizinprodukten für Nischenanwendungen würde in den kommenden zwei Jahren für alle Beteiligten eine Entlastung bringen, ohne die Qualität und Sicherheit der medizinischen Versorgung zu beeinträchtigen.
Der Geltungsbeginn der MDR hat bis jetzt keine schwerwiegenden Folgen für die Gesundheitsversorgung in Deutschland gehabt. Die Hersteller haben sich so gut wie es möglich war, auf den Termin vorbereitet. Aber in den nächsten beiden Jahren müssen Behörden, Anwender und Hersteller von Medizinprodukten gemeinsam dafür sorgen, dass der Rahmen der MDR voll funktionsfähig wird. Nur dann wird die MDR den Beitrag zu mehr Qualität und Sicherheit in der medizinischen Versorgung leisten können, der mit der neuen Verordnung angestrebt wurde.
