17.05.2022
Folge 75: Nur noch 2 Jahre, um Engpässe bei Medizinprodukten auszuschließen
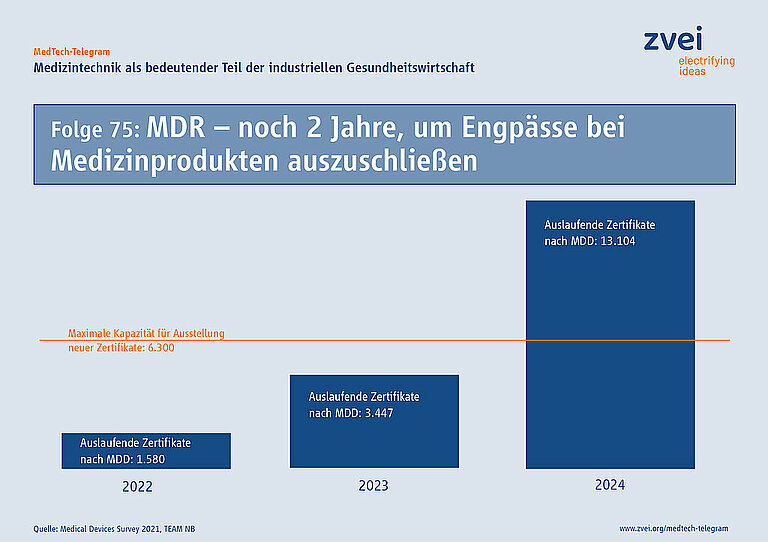
Seit einem Jahr gilt inzwischen die EU-Verordnung für Medizinprodukte (MDR). Alle Medizinprodukte müssen eine Konformitätsbewertung für die CE-Kennzeichnung nach der MDR absolvieren – das gilt auch für sämtliche Bestandsprodukte. Gerade bei diesen besteht nun die Gefahr, dass es in den nächsten beiden Jahren zu Engpässen bei der Versorgung in Deutschland und Europa kommen kann.
Denn noch immer ist das System zur Anwendung der MDR nicht voll funktionsfähig. Behörden, Benannte Stellen und Hersteller müssen dringend gemeinsam daran arbeiten, dass Bestandsprodukte bis spätestens 27. Mai 2024 die erneute Konformitätsbewertung nach der MDR absolvieren können. Derzeit verzögert sich diese erheblich, da es weiterhin nicht ausreichend Benannte Stellen gibt. Zudem fehlen verschiedene Rechtsakte zur Durchführung der MDR. Die Möglichkeit besteht damit, dass viele Zertifikate für Bestandsprodukte auslaufen, bevor eine Konformitätsbewertung nach der MDR möglich ist.
Aktuell ist die Versorgung mit Medizinprodukten nicht gefährdet. Aber: Um die Verfügbarkeit von Bestandsprodukten und damit die Gesundheitsversorgung nachhaltig zu sichern, müssen Behörden und Hersteller in Deutschland und der EU jetzt gemeinsam handeln.
Artikel 120 der MDR regelt, dass Bestandsprodukte weiter nach der bisherigen EU-Richtlinie für Medizinprodukte in Verkehr gebracht werden dürfen, solange die entsprechenden Zertifikate der Benannten Stellen gültig sind. Diese Regelung endet aber spätestens am 27. Mai 2024. Einige Zertifikate können schon vor diesem Datum ihre Gültigkeit verlieren. Wenn bis dahin keine erneute Konformitätsbewertung nach der MDR erfolgt ist, darf das Medizinprodukt nicht mehr in Verkehr gebracht werden und steht dann für die Gesundheitsversorgung nicht mehr zur Verfügung.
