27.03.2023
Folge 91: Wichtige Atempause bei der Anwendung der MDR
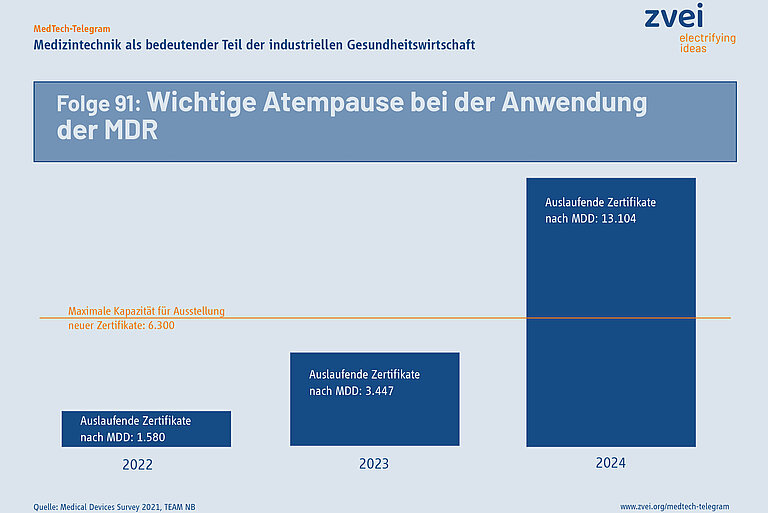
Die Institutionen der Europäischen Union haben in einem beschleunigten Verfahren eine Anpassung der Übergangsfristen der EU-Verordnung über Medizinprodukte (MDR) verabschiedet. Seit der ersten Ankündigung der Europäischen Kommission zu dieser Maßnahme im Dezember 2022 bis zur Verabschiedung durch das Europäische Parlament und den Ministerrat hat es nur knapp drei Monate gedauert. Am 20. März 2023 wurde die Änderung der MDR im Amtsblatt der EU veröffentlicht. Sie ist damit in Kraft getreten und ab sofort anwendbar.
Die schnelle Verabschiedung zeigt, dass Europäische Kommission und Mitgliedstaaten die massiven Probleme bei der Anwendung der MDR erkannt haben. Es ist praktisch unmöglich alle Bestandsprodukte nach früher geltenden EU-Richtlinie über Medizinprodukte bis zum Mai 2024 in die MDR zu überführen. Die jetzt beschlossenen Änderungen sind eine wichtige Atempause bei der Anwendung der MDR auf Bestandsprodukte!
Aber auch bei neu entwickelten Medizinprodukten dauern die Konformitätsbewertungen viel zu lang. Hier droht ein Nachteil für den Medizintechnik-Standort Europa zu entstehen. In den nächsten Monaten müssen deshalb weiterhin pragmatische Lösungen gefunden werden, mit denen die Prozesse rund um die Anwendung der MDR dauerhaft beschleunigt werden können.
Behörden, Benannte Stellen und Industrie müssen ein gemeinsames Verständnis entwickeln, welche Dokumentation und welche Prüfschritte im Rahmen einer Konformitätsbewertung notwendig und ausreichend sind. Dieses Verständnis muss auf europäischer Ebene kommuniziert und durchgesetzt werden.
